신경계 독성의 특징
Neuron은 기본적으로 다른 기관보다 에너지 요구가 많습니다. 뉴런의 주 기능은 전기 신호 전달을 위한 단백질 합성인데, 그 과정에서 에너지 요구가 많기 때문입니다. 뇌가 우리 몸에서 에너지 대사에 차지하는 비율을 생각해보시면 쉽게 이해되실 겁니다.
또한 신경계는 미세한 손상에도 민감합니다. 신경세포 neuron은 자체적으로 물질 대사를 통해 독성 물질을 해독하는 기전이 없고, 지질 성분 많기 때문에 지용성 독성 물질이 축적되기 때문입니다. 게다가 분자량이 작은 지용성 물질이라면 뉴런의 신경세포막, 뇌-혈관 장벽, 혈관을 거의 제한 없이 투과해서 뇌에 도달하지요. 독성 효과가 큽니다.
신경계는 재생이 잘 안 되는 조직이기 때문에 독성 물질에 노출되면 그 효과가 클 수밖에 없습니다.
신경계 독성의 원인
신경계는 저산소증, 저혈당증, 이온 밸런스 장해, 세포골격 손상, 아교세포 손상, 단백질 합성 감소 등에 의해 제 기능을 수행하지 못하게 됩니다.
신경계는 저산소증에 민감합니다. 신경세포 neuron에는 미토콘드리아가 많습니다. ATP 합성을 위해 항상 산소가 공급되어야만 기능을 유지할 수 있습니다. 그래야만 신경전달물질을 합성하고, 분비하고, 회수하고, 전기 신호를 전달할 수 있기 때문입니다.
신경계는 항상 ATP를 합성해야하기 때문에 당을 공급받지 못하면 문제가 발생합니다.
Ion balance disruption 이온 밸런스 이상
세포 내 칼슘 이온이 축적되면 phospholipase나 protease가 활성화되어 미토콘드리아가 손상됩니다. 결국 궁극적으로 신경세포가 죽지요. 더 자세한 내용은 아래에 설명해두었습니다.
칼슘 이온 농도 증가에 의한 세포 손상
https://understandvmedicine.blogspot.com/2022/02/blog-post_27.html
Cytoskeleton damage 세포골격 손상
Axon이나 말초신경이 손상되면 신경이 전달해야할 전기 신호가 제대로 가지 못하겠지요. 신경계가 기능을 상실하는 겁니다.
Protein synthesis 감소
신경세포 neuron은 신경 전달 물질을 합성하고, 분비하고, 회수해야 합니다. 이 모든 과정은 단백질에 의해 조절되어야 합니다. 따라서 단백질 합성이 감소하면 신경계는 기능을 하지 못합니다.
Glial cell damage 아교세포 손상
간이 망가져서 암모니아가 과도하게 축적되면 아교세포가 glutamate를 대사하지 못합니다. 아교세포는 신경계에서 neuron을 제외한 세포들입니다.
Glutamate는 흥분성 신경전달물질인데요, 이를 대사하지 못하고 glutamate가 신경세포 내에 축적되면 문제가 발생합니다. 신경계가 항상 흥분하고 있다면 필요한 전기신호를 필요할 때 전달할 수 없기 때문입니다.
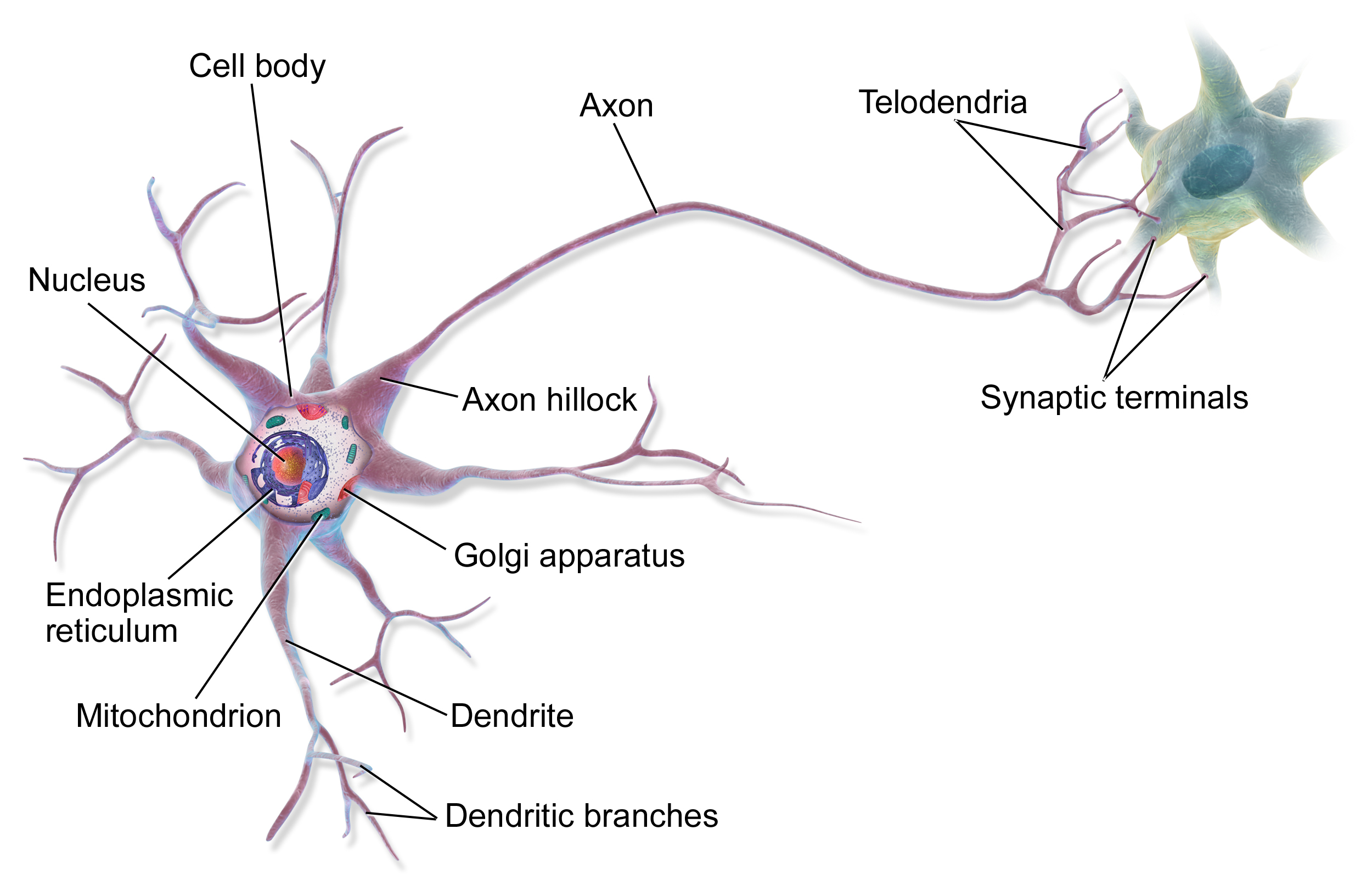
신경계 독성의 결과
신경계를 망가뜨리는 독성 물질은 신경세포 자체를 망가뜨리거나, 축삭을 망가뜨릴 수 있습니다. 전기 신호 전달을 빠르게 해주는 절연체인 수초를 손상시킬 수도 있고, 신경전달을 방해할 수도 있습니다. 혹은 활동 전위를 랜덤하게 만들어 근육이 떨리게할 수도 있고, 전기 전도가 제대로 일어나지 못하게 할 수 있습니다.
Axonopathy
Axonopathy는 독성 물질이 축삭Axon의 전도에 영향을 주는 경우를 말하는 용어입니다. 임상 증상(마비)이 느리게 나타나며 비가역적입니다. 즉, 축삭이 손상되면 회복될 수 없는 마비가 일어납니다.
Myelinopathy
CNS에선 oligodendrocyte, PNS에선 Schwann cell가 절연체(수초, myelin sheath)를 형성하고 있지요.
지용성 물질인 triethyltin, hexachlorophene와 일부 탄화수소는 수초의 지질 성분과 결합합니다. 절연체인 수초의 구조가 변형되면 신경의 전기 신호가 제대로 전달되지 않습니다.
이제 각각의 물질들이 어떻게 신경계를 손상시키는지 하나씩 살펴보겠습니다.
수은
수은은 대표적인 신경계 독성 물질입니다. 수은은 SH기와 잘 결합합니다.
미토콘드리아의 효소 중에는 SH기를 함유한 효소가 많기 때문에 신경계는 수은에 매우 취약합니다. 수은이 미토콘드리아의 효소들과 결합하면 효소의 전자 분포가 바뀌어 다른 구조로 변형이 되고 결과적으로 제 기능을 수행하지 못하기 때문입니다. 미토콘드리아는 에너지 대사를 담당하는 세포소기관이지요. 신경계는 특히 에너지 요구량이 많기 때문에 수은에 취약합니다.
중추신경계를 흥분시키는 물질
AchE 억제 살충제
살충제 중 AchE 억제제들은 발작을 유도합니다. 아세틸콜린은 부교감신경, 운동신경 등을 흥분시키는 물질입니다. 아세틸콜린 분해효소를 억제하면 신경계 내에 아세틸콜린이 축적되고, 그 결과 근육의 발작이 일어납니다.
Antihistamine 항히스타민
항히스타민제는 저용량에서는 신경계를 억제하고 고용량에서 신경계를 흥분시키는 흥분제입니다. 이는 히스타민의 다양한 기능과 관련이 있습니다. 히스타민에 대해서는 다음에 다뤄보겠습니다.
methylxanthine 메틸잔틴
저용량에서는 억제제이고 고용량에서 흥분제입니다. 커피의 카페인을 생각하시면 됩니다. 카페인을 비롯한 메틸잔틴 물질들은 아데노신이 아데노신 수용체와 결합하는 것을 차단합니다. 그 결과 신경계가 흥분 상태로 유지됩니다.
카페인은 Adenosine 수용체를 차단하고 phosphodiesterase를 차단합니다. 그 결과 신경세포 내에 cAMP 농도가 증가하고 cAMP가 증가한 뉴런은 카테콜아민(도파민, 에피네프린 등)을 많이 분비합니다.
Cocaine
코카인은 카테콜아민(도파민, 에피네프린 등)의 재흡수를 억제합니다. 그 결과 중추신경계에 카테콜아민 농도가 높아지고, 중추신경계는 흥분합니다.
중추신경계를 억제하는 물질

유기수은
수은은 생명체 내(특히 해양 미생물)에서 대사되어 유기수은이 됩니다. 유기수은은 배설되지 못하고 체내에 축적되는 대표적인 물질이지요.
해양 미생물이 수은을 유기수은으로 대사하면 그것을 물고기가 먹다가 결국 사람이 물고기를 먹어 사람에 중독 증상이 일어납니다. 특히 참치, 고등어, 삼치와 같은 어류들은 위험할 수 있습니다.
유기수은의 증상은 마비입니다.
더 자세한 내용은 수은의 독성 편에서 설명했습니다.
https://understandvmedicine.blogspot.com/2021/10/blog-post_23.html
시냅스 전달을 억제하는 물질
어떤 독성 물질들은 신경전달물질의 활성화를 방해합니다. 보툴리늄 독소(보톡스), 파상풍균의 독소 등은 시냅스에서 신경 전달 물질이 전달되는 과정을 차단하지요.
Botulism toxin(Botox)
보툴리늄 독소(보톡스)는 아세틸콜린이 분비되지 못하게 하는 물질입니다. Clostridium botulinum이라는 혐기성 세균이 합성하는 독소입니다. 혐기성 환경인 통조림, 꿀 등을 먹을 때는 특히 주의해야 하지요.
신경과 근육의 연접부에서 근육에 신호를 전달해주는 물질이 아세틸콜린이기 때문에 보툴리늄 독소에 중독되면 마비가 일어납니다. 특히 호흡에 필요한 호흡근이 마비되면 사망합니다.
단, 보툴리늄 독소는 뇌-혈관 장벽을 통과하지 못해서 뇌에서는 효과가 미미합니다.
Tetanus 파상풍 독소
Clostridium tetani라는 세균이 생산하는 파상풍 독소는 GABA-gated Cl- channel을 억제하여 과도한 흥분을 일으키는 물질입니다.
이 독소에 의해 신경 세포 내부로 Cl- 음이온이 들어오지 못하면 신경세포에 음이온과 양이온의 비율이 깨집니다. 즉, 신경세포 세포막의 안쪽 전위가 높아지게 유도하는 물질이지요. 신경세포 내부에 양이온이 많아지면 신경세포는 흥분합니다.
신경계 흥분에 의해 근육이 흥분하고 그 결과 전신의 근육이 수축합니다. 동물은 몸을 굽히는 근육보다는 몸을 펴는 근육이 보통 더 강합니다. 그 결과 전신이 빳빳하게 펴집니다. 따라서 후궁반장, 발작 증상이 일어납니다.
Action potential을 생성하거나 흥분 전도를 방해하는 물질
몇몇 신경계 독성물질은 활동 전위가 생성되거나 전도되는 과정을 방해하기도 합니다.
우선, 활동 전위가 어떻게 전달되는지 그 원리를 간단하게 정리해봅시다.
Na : action potential 시작은 Na+ 이온의 급격한 유입입니다.
K : 그 다음 세포 밖으로 K+ 이온의 유출이 나타납니다.(느리게 시작)
Cl : Cl- 이온의 역할은 막전위를 유지하는 것입니다.
Ca : 칼슘이온은 휴지 막전위와 역치를 유지하는 양이온입니다.
살충제인 DDT와 pyrethrin은 Na, K 이동에 영향을 주는 독성 물질이지요.
DDT
DDT는 신경세포막의 K+ 이온 운반체를 감소시키고 Na+ 이온 통로를 닫습니다. 그 결과 Na-K ATPase와 Ca-Mg ATPase가 억제됩니다. 즉, 세포 내부에 칼슘 이온 농도가 증가합니다. 세포 내부에 칼슘 이온 농도가 증가하면 Calmodulin과 Ca2+ 복합체가 형성됩니다. 이 복합체는 신경세포 내부에 저장되어있던 신경전달물질을 방출시킵니다.
Pyrethrin 살충제
Pyrethrin은 Na+ channel에 작용하여 비정상적인 action potential을 생성합니다.
또한 Ca-Mg ATPase를 억제하여 DDT와 마찬가지 원리로 신경전달물질을 방출시킵니다. 그 결과 비정상적인 탈분극이 발생하여 발작 증상이 나타납니다.
Pyrethroid 살충제
Pyrethroid 살충제는 receptor site에서 baga, glutamate binding 장애를 일으킵니다.
발작을 일으키는 물질
Amphetamine
암페타민은 카테콜아민(도파민, 에피네프린 등)을 방출시킵니다. 그 정도가 과도할 때 발작이 일어납니다.
4-ammopyridine
아세틸콜린을 방출시키며, K+ 이온에 의한 재분극을 방해하는 물질입니다. 따라서 신경계가 계속 흥분된 상태가 되고 결과적으로 발작이 일어납니다.
Bromethalin
Bromethalin은 산화적인산화를 방해하여 에너지 부족 상태를 유발합니다. 그 결과 신경세포의 이온 펌프가 작동하지 못합니다.
-> 저농도에서는 우울, 무기력을 유발하고 고농도에서는 발작을 일으킵니다.
Ammonia
Bromethalin과 마찬가지로 발작을 일으킵니다.
중추신경계에 부종을 일으키는 물질
Cyanide 시안화물(청산)
Cyanide는 Cytochrome 산화효소를 억제합니다. 신경세포는 에너지 요구량이 높은데 cyanide에 의해 전자전달계가 제대로 작동하지 못합니다. 그 결과 에너지 부족에 의해 삼투압으로 세포 내부에 물이 들어오는 것을 막을 수 없습니다. 뇌에 부종이 생깁니다.
Fluoroacetate
Fluoroacetate는 TCA cycle에서 aconitase를 억제하는 물질입니다. 역시 ATP를 합성하지 못하고 에너지 부족에 의해 뇌에 부종이 생깁니다.
Hexachlorophene, Nitrofurazone
Hexachlorophene과 nitrofurazone은 미토콘드리아 내부에서 일어나는 산화적인산화를 방해합니다. 마찬가지로 ATP 합성에 문제가 생겨 부종이 생깁니다.
어린 송아지가 특히 매우 취약하다고 알려져있습니다.
우울을 일으키는 물질
Alcohol
알코올은 분자량이 작고 지용성인 물질입니다. 분자량이 작고 지용성 물질이기 때문에 세포막 인지질을 쉽게 통과합니다. 지용성 물질이기 때문에 여러 생체막을 통과할 뿐만 아니라 수용성 물질이기 때문에 혈액 속에 녹아 뇌에 쉽게 도달합니다. 신경세포의 세포막과 결합하여 세포막의 투과성을 증가시키는 일종의 마취제입니다. 우울을 유발합니다.
Barbiturate
Barbiturate는 GABA와 유사한 물질로, 신경계가 흥분하지 못하도록 하는 마취제입니다. 우울을 일으킵니다.
경련을 일으키는 물질
Tremor(진전), tetany(강직성 근경련)은 일종의 대사 장애입니다. Seizure(발작)와는 다르게 전신에 대칭적으로 일어납니다.
유기인제와 carbamate 살충제는 cholinesterase를 억제하여 아세틸콜린이 신경계 내에 축적되게 합니다. 아세틸콜린을 인식하는 니코틴성 수용체(nicotinic receptor)를 과도하게 흥분시켜서 경련을 일으킵니다.
마비를 일으키는 물질
Botulinum toxin은 아세틸콜린의 방출을 억제하는 물질로 마비를 일으킵니다.
Black widow spider라는 거미의 거미독은 아세틸콜린과 아드레날린을 고갈시켜서 마비를 일으킵니다.
Curare는 근육을 마비시키기 위한 약으로, cholinergic receptor 억제제입니다. 마비를 일으킵니다.
기타 신경계 독성 물질
Carbon monoxide : carboxyhemoglobin 생성 -> anoxia -> necrosis of neuron
Fumonisin : sphinganine이 sphingosine으로 전환되는 대사를 억제하는 물질입니다.
Hydrogen sulfide : cytochrome C oxidase 억제 -> 전자전달계 억제
Ivermectin : GABA 생성 촉진, GABA binding 억제…. Collies 취약(BBB 통과함)
납 : GABA 억제
알킬수은 : sulfhydryl enzyme의 단백질 합성 방해
Opioid(morphine, codeine) : 많은 리셉터와 상호작용
Atropine : Ach receptor의 경쟁적 저해 -> seizure, anticholinergic
Carbamate insecticide : cholinesterase와 결합 -> cholinesterase inhibition




.png)
/eosinophil-white-blood-cell-leukocyte-400x-at-35mm-human-blood-smear-eosinophils-have-a-bilobed-nucleus-and-large-reddish-cytoplasmic-granules-increased-numbers-of-eosinophils-eosinophilia-occur-in-allergies-1-3-of-the-total-of-white--58ac65cd5f9b58a3c918b494.jpg)